Các bệnh nhân ung thư đại trực tràng di căn nay đã có thể lựa chọn phác đồ điều trị mới. Cơ quan Quản lý Dược phẩm & Thực phẩm Hoa Kỳ (FDA) vừa phê duyệt thuốc nhắm trúng đích Encorafenib (tên thương mại là Braftovi) kết hợp với một thuốc nhắm trúng đích khác là Cetuximab (Erbitux) để điều trị ung thư đại trực tràng.
Encorafenib (Braftovi) đã được phê duyệt để điều trị cho một số bệnh nhân ung thư đại trực tràng, bao gồm cả phác đồ kết hợp với Cetuximab (Erbitux) điều trị bệnh nhân người lớn bị ung thư đại tràng di căn có đột biến V600E ở gene BRAF và bệnh nhân đã từng điều trị ít nhất một phác đồ khác.
Cả 2 loại thuốc này đều là thuốc nhắm trúng đích. Cetuximab nhắm vào protein EGFR, đã từng được phê duyệt để điều trị bệnh nhân ung thư đại trực tràng. Lần này được bổ sung kết hợp với Encorafenib nhắm đến BRAF protein để điều trị bệnh nhân ung thư hắc tố có đột biến gene BRAF.
Phác đồ mới được phê duyệt căn cứ vào kết quả thực nghiêm lâm sàng giai đoạn 3 ở quy mô lớn (BEACON CRC) do hãng dược phẩm Pfizer tài trợ.
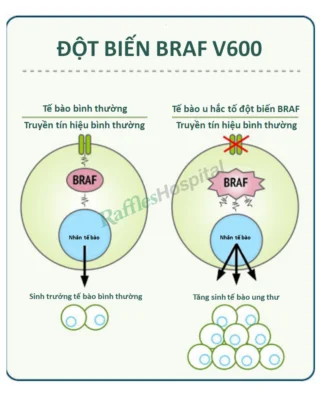
Đột biến V600E ở gene BRAF được phát hiện ở khoảng 10% bệnh nhân ung thư đại trực tràng và thường liên quan tới tiên lượng xấu. Theo chuyên gia của Viện Ung thư Hoa Kỳ, bệnh nhân thuộc nhóm này không đáp ứng với các phác đồ đã có. Đặc tính ức chế BRAF đã được chứng minh có hiệu quả hạn chế ở bệnh nhân ung thư đại trực tràng đột biến BRAF. Tuy nhiên, chuyên gia giải thích thêm “Nếu chỉ ngăn chặn BFAF – là tác nhân nguyên phát của ung thư, tế bào ung thư có thể nhận diện được & tìm cách tránh tác dụng của thuốc”.
Chương trình thực nghiệm BEACON CRC được thực hiện để đánh giá hiệu quả của phác đồ kết hợp các thuốc nhắm trúng đích trong việc ngăn chặn các thành phần khác nhau của đường truyền tín hiệu BRAF, nhằm tăng hiệu quả điều trị bệnh nhân ung thư đại trực tràng di căn có đột biến BRAF.
Các chuyên gia của chương trình đã so sánh phác đồ kết hợp 3 loại thuốc đích (Encorafinib, Cetuximab và Binimetinib “Mektovi”) và phác đồ 2 loại thuốc (Encorafinib, Cetuximab) với phác đồ hóa trị tiêu chuẩn kết hợp với Cetuximab (nhóm chứng). Cả 2 phác đồ thực nghiệm đều cho kết quả vượt trội so với phác đồ tiêu chuẩn, trong đó phác đồ kết hợp 2 loại thuốc đích có hiệu quả tương đương kết hợp 3 loại.
So với nhóm chứng, bệnh nhân điều trị với Encorafenib kết hợp Cetuximab thời gian sống trung vị tăng khoảng > 50%, đồng thời kích thước khối u giảm 20% so với 2% ở nhóm chứng.
Chương trình thực nghiệm này “dạy cho chúng ta biết cách sủ dụng các phác đồ điều trị đích”.
Tác dụng phụ nghiêm trọng của phác đồ kết hợp Encorafenib & Cetuximab chủ yếu là mệt mỏi & suy nhược. Các phản ứng thường gặp khác gồm có buồn nôn, nổi mẩn trên da & tiêu chảy.
Nguồn: cancer.gov
.png)
Thông tin liên hệ (Hỗ trợ tư vấn và phiên dịch miễn phí)
VĂN PHÒNG ĐẠI DIỆN RAFFLES TẠI TP. HỒ CHÍ MINH
Địa chỉ: 167A Nam Kỳ Khởi Nghĩa, Phường 7, Quận 3, TP. Hồ Chí Minh
Điện thoại: +84-28 3822 6086/ +84-28 3822 6087
Di động: +84 947 815 338 (Ms.Thuến) / +84 912 175 162 (Ms. Thủy)
Email: hcm@rafflesmedical.com
VĂN PHÒNG ĐẠI DIỆN RAFFLES TẠI HÀ NỘI
Địa chỉ: 51 Xuân Diệu, Quận Tây Hồ, TP. Hà Nội (phía sau Fraiser Suites)
Điện thoại: +84-24 3676 2222
Di động: +84 941 978 228 (Ms. Hương) / +84 936 328 588 (Ms. Lan Anh)
Email: hanoi@rafflesmedical.com



